الكادميوم ، مؤتمر نزع السلاح ، العدد الذري 48
سعر الكادميوم ، التاريخ ، الحدوث ، الاستخراج والاستخدام
الكادميوم (أيضًا نادرًا الكادميوم ، اليونانية mαδμία kadmía ، الكادمي اللاتيني ، "أرض الزنك المحتوية على أكسدة أو كربونات") عنصر كيميائي مع رمز العنصر Cd والرقم الذري 48. عادةً ما يتم حسابها بين الفلزات الانتقالية ، على الرغم من أن لها قشرة د مغلقة وبالتالي تشبه عناصر المجموعة الرئيسية ، وخاصة الفلزات القلوية الأرضية. في الجدول الدوري يكون في 5. فترة وكذلك 2. مجموعة فرعية (مجموعة 12) أو مجموعة الزنك.
قصة
اكتشف 1817 الكادميوم بشكل مستقل في كربونات الزنك الملوثة بواسطة فريدريش سترومير وكارل صموئيل هيرمان. لاحظ Stromeyer أن كربونات الزنك الملوثة غير مشبعة بالتسخين - وهو سلوك لم يظهر كربونات الزنك النقي. منذ ما يقرب من سنوات 100 ، تم الفوز بالمعادن في ألمانيا فقط.
بليني الأكبر ذكرت في تقريرها كتب حوالي عام 77 التاريخ الطبيعي الحالة الطبيعية تاريخ شعب من Galmeifunden في ألمانيا: "Cadmea [...] ferunt nuper etiam في ألمانيا في Provincia repertum" (الألمانية: "في الآونة الأخيرة تم العثور في محافظة ألمانيا كالامين"). وقد استخدم مصطلح الكادميوم منذ العصور الوسطى، ويفترض لالزنك أو Karbonaterz. كما يمكن أن ينظر إليها من قبل الامبراطور فريدريك الثاني. وفي أبريل 1226 في رافينا أصدرت الشهادة، التي تمنح دير البينديكتين القديس بولس في وادي Lavant حق واحد "التحرير Cadmiae تام argentj quam plumbi آخرون من الحديد، كيو في في Territorio ipsius monasteri دي Cetero inveniri contigerint إعلان التأليف الخنزيري "(الألمانية:" أن يتم استخدام الزنك والفضة والرصاص والحديد، التي وجدت في منطقة الدير لأغراض ").
على الرغم من سمية الكادميوم ومركباته ، فقد ثبت أن المخطوطة الصيدلانية البريطانية الخاصة بـ 1907 تستخدم يوديد الكادميوم كعلاج لل الدعك (الغدد اللزجة) والغدد الصماء (الغدد اللينة).
1907 تعريف الاتحاد الفلكي الدولي انغستروم كما العصر 1 / 6438,4696 الطول الموجي للخط طيفي أحمر الكادميوم في الهواء الجاف مع محتوى ثاني أكسيد الكربون من 0,03٪ عند درجة حرارة 15 ° C وضغط 1 أجهزة الصراف الآلي. المؤتمر العام للأوزان والمقاييس المقبولة في الأوقات 1960 1.553.164,13 الطول الموجي للخط طيفي أحمر الكادميوم كتعريف الثانوي من المتر.
استخدمت 1942 صفائح الكادميوم Enrico Fermi في أول مفاعل نووي في العالم. يمكن دفع الأوراق داخل وخارج المفاعل للتحكم في تفاعل السلسلة. يمكن للكادميوم التقاط النيوترونات ذات الفجوة المتوسطة وبالتالي التأثير على أهمية المفاعل.
ظهور
الكادميوم عنصر نادر جدًا. تبلغ حصتها في قشرة الأرض حوالي 3 · 10 فقط-5 . الكادميوم نادر للغاية في شكله الطبيعي ، أي في شكله الأولي. حتى الآن لم يُعرف سوى خمسة مواقع في ثلاثة بلدان: نهر خانية في حوض فيليوي ، وحوض نهر جانا بالقرب من فيرخويانسك ، وتطفل بيليخ في جمهورية ساخا الروسية (ياقوتيا ، شرق سيبيريا) ؛ حفر Goldstrike بالقرب من Lynn في مقاطعة Eureka في ولاية نيفادا الأمريكية وكتلة Burabaiskii في منطقة Akumola في كازاخستان.
عندما الخامات التي تحتوي على الكادميوم وخصوصا مصراع الكادميوم Greenockit (CDS) مع ما يصل الى 77,81٪ الكادميوم وCadmiumspat otavite (CdCO3) معروفة حتى 65,20٪ الكادميوم، ولكن هذه هي نادرة جدا للتعدين التجاري. كلاهما دائما تقريبا (ZnCO3) مع مختلف خامات الزنك مثل سفاليرايت (ZnS) وسميثسونيت اجتماعيا.
كليًا حتى الآن (قف 2018) شيء أكثر من معادن 20 للكادميوم معروفة. يحتوي أكسيد الكادميوم النادر للغاية في مونتيبونيت على أعلى نسبة من محتوى الكادميوم تصل إلى 87,54٪. المعادن الأخرى تشمل Hawleyit (77,81٪ Cd) ، Cadmoselite (58,74٪ Cd) و Drobecit (IMA 2002-034 ، 40,07٪ Cd).
الكادميوم كمعدن
تم وصف الكادميوم الذي يحدث بشكل طبيعي في شكله الأولي لأول مرة بواسطة 1979 BV Oleinikov و AV Okrugin و NV Leskova. ومعترف بها من قبل الرابطة الدولية للمعادن (IMA) كنوع معدني مستقل (رقم الوصول الداخلي IMA: 1980-086a).
وفقًا لتصنيف المعادن وفقًا لنموذج Strunz (إصدار 9) ، فإن الكادميوم يخضع لنظام لا. 1.AB.05 (عناصر - المعادن والفلزات - عائلة الزنك والنحاس الأصفر - مجموعة الزنك). في 8 عفا عليها الزمن. ومع ذلك ، لم يتم إدراج الكادميوم بعد في إصدار Strunz's Mineral Systematics. فقط في آخر 2018 المحدث "دليل Lapis المعدنية" ، والذي يعتمد على هذا الشكل من نظام الترقيم نظرًا لهواة الجمع والمجموعات المؤسسية الخاصة ، تلقى المعدن النظام والرقم المعدني. I / A.4-40. يؤدي تصنيف المعادن وفقًا لـ Dana ، والذي يستخدم في الغالب في البلدان الناطقة باللغة الإنجليزية ، إلى عنصر العناصر المعدنية وفقًا للنظام رقم. 01.01.05.02.
استخراج والعرض
يتم الحصول على الكادميوم حصريًا كمنتج ثانوي لصهر الزنك ، وبدرجة أقل ، صهر الرصاص والنحاس. تنطبق كميات أصغر أيضًا على إعادة تدوير الحديد والصلب.
يعتمد إنتاج الكادميوم على كيفية استخراج الزنك. في استخراج الزنك الجاف ، يتم تقليل الكادميوم أولاً مع الزنك. لأن الكادميوم لديه نقطة غليان أقل من الزنك ، فإنه يتبخر بسهولة أكبر. نتيجة لذلك ، يتبخر خليط الكادميوم والزنك من وعاء الاختزال ويتفاعل في مكان آخر مع الأكسجين إلى الكادميوم وأكسيد الزنك. بعد ذلك ، يتم خلط هذا الخليط في وعاء تقطير مع فحم الكوك ويتم تقطيره من الكادميوم من الزنك. يسمح التقطير التجزيئي بتحقيق مستويات أعلى من الكادميوم.
أثناء استخراج الزنك الرطب ، يتم تقليل أيونات الكادميوم الذائبة وترسبها بواسطة غبار الزنك. يتأكسد الكادميوم الناتج بالأكسجين إلى أكسيد الكادميوم ويذوب في حامض الكبريتيك. يتم الحصول على محلول سلفات الكادميوم الناتج عن طريق التحليل الكهربائي باستخدام أنودات الألمنيوم وكاثودات الرصاص خاصة كادميوم الإلكتروليت النقي.
الخصائص الفيزيائية
الكادميوم هو معدن لامع فضي بكثافة 8,65 g / cm3. أنها لينة (Mohs صلابة 2) ، تشوه plastically ويمكن أيضا أن تقطع بسكين لسحب الأسلاك والمطرقة في المنشورات.
يصلب الكادميوم حصريًا في نظام الكريستال السداسي في المجموعة الفضائية P63 / mmc (رقم المجموعة الفضائية 194). المعلمات شعرية الكادميوم النقي هي = 0,2979 نانومتر (يتوافق مع 2,98 Å) و c = 0,5617 نانومتر (يتوافق مع 5,62 Å) لوحدات الصيغة 2 لكل خلية وحدة.
على غرار القصدير ، تحدث الضوضاء النموذجية عند ثني الكادميوم ذو النقاء المتوسط (يُسمى القصدير بيوتر في القصدير). الكادميوم المصقول يفقد لمعانه في الهواء بعد بضعة أيام ، حتى لو كان أكثر مقاومة للتآكل من الزنك. في الهواء المكربن ، فإنه يشكل طلاء أبيض رمادي ، يحتوي على ثاني أكسيد الكربون. يتم تسخينه بشدة ، وهو يحترق من لهب أصفر إلى لهب أصفر إلى ثاني أكسيد الكادميوم أكسيد الكادميوم.
تم اختبار CdO لسمية عالية خلال الحرب العالمية الثانية من قبل الولايات المتحدة لمدى ملاءمتها كعامل الحرب الكيميائية.
الخواص الكيميائية
في المركبات الكيميائية عادة ما يكون ثنائي التكافؤ. إنه مشابه كيميائيًا للزنك ، ولكنه يميل إلى تكوين مركبات معقدة برقم التنسيق 4. في الهواء الكادميوم يشكل سواد السطح بسبب الأكسدة. في الوسط القلوي ، السطح غير قابل للذوبان ، ثقيل بحمض الكبريتيك وحمض الهيدروكلوريك ، وقابل للذوبان بسهولة في حمض النتريك.
استعمال
بسبب ارتفاع سمية الكادميوم أهميته يتناقص. منذ ديسمبر 2011 محظور في المجوهرات والسبائك لحام و PVC في الاتحاد الأوروبي. الكادميوم مستخدم أو تم استخدامه:
- كحماية من التآكل للمواد الحديدية (طلاء الكادميوم)
- كما طلاء السطح لمواد الألومنيوم في الهندسة العسكرية (مثل قاذفات الصواريخ)
- لبطاريات النيكل والكادميوم
- للأصباغ الملونة من الأصفر إلى الأحمر الداكن من كبريتيد الكادميوم وسيلينيد الكادميوم للدهانات والبلاستيك (وفي الوقت نفسه أهمية عملية منخفضة بسبب المخاطر الصحية المحتملة ، وخاصة عند حرق المواد المقابلة)
- كمعادن السبائك في السبائك المنخفضة الصهر ، على سبيل المثال مواد تحمل أو معادن Wood
- في وقت سابق من مواد التشحيم في أقراص الفرامل
- كمكون من مواد لحام (لحام) ، وأيضا لسبائك مختلط
- لإنتاج أشباه الموصلات
- أكسيد الكادميوم كفوسفور في أنابيب التلفزيون بالأبيض والأسود وإضافة في الفوسفور الأزرق والأخضر للأنابيب الملونة
- أكسيد الكادميوم كخليط للفضة في تبديل الاتصالات
- كمادة واقية ضد النيوترونات الحرارية وقضبان التحكم في التكنولوجيا النووية بسبب المقطع العرضي العالي بشكل خاص لنظير 113 لالتقاط النيوترون
- كمصدر لإشعاع غاما عالي الطاقة (حول 7 MeV) من النيوترونات الحرارية للجيل الأخير من البوزيترونات من خلال توليد زوج
- كبريتيد الكادميوم في عدادات التعرض التي تشبه حساسيتها الطيفية حساسية العين البشرية
- الكادميوم تيلورايد كمستشعر حساس للأشعة تحت الحمراء للكاميرات (صفائف المستوى البؤري)
- في الخلايا الشمسية ذات الأغشية الرقيقة مثل تلوريد الكادميوم أو كبريتيد الكادميوم لتوليد الطاقة
- الكادميوم ستيرات كمثبت في المواد البلاستيكية ، على سبيل المثال في PVC (غير حساس للضوء ، ولكن في هذه الأثناء ذات أهمية عملية منخفضة بسبب المخاطر الصحية المحتملة)
- في وقت سابق في عناصر ويستون العادية لتحديد وحدة قياس الجهد ، فولت 1
- سبائك البزموت الكادميوم لالصمامات
- سبائك الفضة والكادميوم كمادة مزيلة للأكسدة في إنتاج الفضة الاسترليني
- للمجوهرات: سبائك الذهب والكادميوم الذهب الأخضر
- مصباح الكادميوم
- ليزر الهليوم والكادميوم
- أيونات الكادميوم لمنع قنوات الكالسيوم تفعيلها الجهد في الفيزيولوجيا الكهربية
لتلوين الزجاج باللون الأصفر والبرتقالي والأحمر بإضافة كبريتيد الكادميوم والسيلينيد والتيلورايد أو مخاليط منه.
إن أشباه الموصلات من النوع الثاني إلى السادس تعتبر مركبات كبريتيد الكادميوم ، كبريتيد الكادميوم (الأصفر) ، سيلينيد الكادميوم (الأحمر) ، والكالسيوم تيلورايد (أسود). يتم إنتاجها ، على سبيل المثال ، الجسيمات النانوية كنقاط الكم (النقاط الكمومية) وتستخدم ، في جملة أمور ، في الكيمياء الحيوية في المختبر.
دليل
كعينة أولية للكادميوم ، يمكن تقديم ما يسمى Glühröhrchenprobe. لهذا الغرض ، يتم تسخين بعض المواد المخزنة في Glühröhrchen عالي الانصهار وتقليل خليط أكسيد الكبريت الناتج مع أكسالات الصوديوم إلى المعادن. كمكون متقلب ، يتبخر الكادميوم ويتراكم كمرآة معدنية في الجزء العلوي من الأنبوب.
من خلال إضافة الكبريت لاحقًا وتجديد الصلب ، يتشكل كبريتيد الكادميوم من المرآة المعدنية وبخار الكبريت ، وهو اللون الأحمر في الحرارة والأصفر في درجة حرارة الغرفة. هذا اللون يمكن أن يتكرر عدة مرات.
رد فعل الكشف عن كاتيونات الكادميوم هو هطول الأمطار بمحلول كبريتيد أو كبريتيد الهيدروجين مثل كبريتيد الكادميوم الأصفر. تتداخل أيونات المعادن الثقيلة الأخرى مع هذا الاكتشاف ، وذلك قبل إجراء الفصل الكاتيوني.
من أجل التحديد الكمي للآثار الكادميوم ينصح الاستقطاب. تدخل أيونات الكادميوم (II) مستوى في 1 M KCl في -0,64 V (مقابل SCE). في نطاق التتبع الفائق ، يمكن استخدام قياس الجهد العكسي على أقطاب الزئبق. حساسة جدا أيضا أنبوب الجرافيت AAS من الكادميوم. هنا ، لا يزال بالإمكان اكتشاف 0,003 ميكروغرام / لتر. العنصر المتطاير نسبيا لا يتحمل درجة حرارة الانحلال الحراري العالية. يمكن لمعدّل المصفوفة مثل نترات المغنيسيوم البلاديوم أن يساعد.
سلامة
الكادميوم شديد السمية وتصنف مركباته على أنها ضارة (مثل الكادميوم تيلورايد) أو سامة (مثل كبريتيد الكادميوم) أو شديدة السمية (أكسيد الكادميوم) ؛ هناك أيضا شك معقول من وجود تأثير مسرطنة في البشر. الغبار المحتوي على الكادميوم يسبب أضرارًا في الرئتين والكبد والكليتين.
في مناطق العمل التي تستخدم فيها مركبات الكادميوم المسخنة (محطات اللحام وحمامات الكادميوم) ، تأكد من التهوية الجيدة أو الاستخراج. وفقًا لمرسوم الحظر الكيميائي ، يجب ألا يتجاوز محتوى الكادميوم في البلاستيك 0,01 في المئة بالوزن (100 mg / kg). ينطبق هذا الحد في جميع أنحاء الاتحاد الأوروبي.
منذ ديسمبر / كانون الأول ، تطبق 2011 حظراً أكثر صرامة على الكادميوم في المواد البلاستيكية والدهانات والمثبتات ومعالجة معينة للمعادن وفقًا لوائح REACH ، وأدخل 23 في الملحق السابع عشر. في السابق ، كان النحاس المختلط يحتوي عادةً على 10٪ إلى 25٪ كادميوم ، مجوهرات للأطفال حتى 30٪ ، PVC 0,2٪. مع 10. في ديسمبر 2011 ، تم تمديد الحظر المفروض على الجنود المحتجزين على الكادميوم في لحام وإنتاج وتسويق المجوهرات المطلية بالكادميوم. بالإضافة إلى ذلك ، تم أيضًا تضمين جميع المنتجات المحتوية على الـ PVC ، باستثناء إعادة تدوير الـ PVC. مع التنظيم (الاتحاد الأوروبي) 2016 / 217 من 16. في فبراير 2016 ، تمت إضافة الكادميوم في بعض الدهانات والورنيش إلى إدخال 23 في الملحق السابع عشر من لائحة REACH. بالإضافة إلى ذلك ، كان محتوى الكادميوم في بعض الدهانات والورنيش المحتوي على الزنك أو المنتجات المحتوية عليه محدودًا. هناك استثناءات ، على سبيل المثال بسبب كثافة الطاقة العالية لبطاريات Ni-Cd في الأجهزة الكهربائية اللاسلكية.
علم السموم
الكادميوم هو نتاج ثانوي لا يمكن تجنبه من استخراج الزنك والرصاص والنحاس في الصناعة الكيميائية. كما يمكن العثور على الكادميوم في الأسمدة والمبيدات الحشرية.
تسجيل والمخاطر
لقد خفضت منظمة الصحة العالمية مرارًا وتكرارًا بيانها بشأن تناول الكادميوم بشكل مقبول في السنوات الأخيرة ، وآخرها 2013 إلى مدخول شهري مقبول (TMI) يبلغ 25 ميكروغرام لكل كيلوغرام من وزن الجسم. أصدرت هيئة سلامة الغذاء الأوروبية 2009 بمستوى أقل بكثير من 2,5 ميكروغرام لكل كيلوغرام من وزن الجسم المسموح به الأسبوعي (TWI).
يمتص البشر الكادميوم من خلال الطعام. الأطعمة الغنية بالكادميوم تشمل: الكبد ، الفطر ، المحاريات وغيرها من المحاريات ، ومسحوق الكاكاو والأعشاب البحرية المجففة. بالإضافة إلى ذلك ، يحتوي بذور الكتان على الكثير من الكادميوم ، ولهذا يوصى بعدم تناول 20 جم من بذور الكتان يوميًا. بالإضافة إلى ذلك ، منذ إدخال الأسمدة الصناعية ، كان هناك تراكم للكادميوم على الأراضي الزراعية وبالتالي في جميع الأطعمة تقريبًا. موارد الفوسفات محدودة ، ومعظم الموارد ملوثة بالكادميوم أو المعادن الثقيلة المشعة. محتوى الكادميوم من رواسب الفوسفات هو مختلف جدا. لقد أدخلت العديد من البلدان الصناعية بالفعل حدًا للكادميوم في الأسمدة. يقتصر تركيز الكادميوم في النمسا على 75 mg / kg P2O5. أيضًا ، ينقل دخان التبغ كميات كبيرة نسبيًا من الكادميوم إلى الرئتين ، حيث ينتشر بالدم في الجسم.
لا سيما الأشخاص الذين يعملون في مصانع الكادميوم عالية في خطر متزايد. ولكن هناك أيضا مخاطر من المقالب البرية والأشغال المعدنية. استنشاق الكادميوم يمكن أن يلحق أضرارا بالغة بالرئتين ويؤدي إلى الموت إن الحوادث في الصناعة - كما هو الحال في مقاطعة قوانغدونغ الصينية - وعقود من الانبعاثات - كما في حالة مرض إيتاي إيتاي (عند البشر) ومرض غرينيشر (في رعي الماشية) - توضح المخاطر الحقيقية.
الضرر في البشر
يمكن أن يتراكم الكادميوم تدريجياً في الجسم لأسباب صناعية أو بيئية ويسبب تسممًا مزمنًا يصعب التعرف عليه.
يمتص الكادميوم من النظام الغذائي إلى حوالي 5 ٪ في الأمعاء. مع نقص الحديد والكالسيوم ، يزداد معدل الامتصاص ، مما يشير إلى أن جميع المعادن الثلاثة تستخدم نفس مسار النقل. يحفز الكادميوم أولاً في الكبد تخليق الميتالوثيونين ، الذي يشكل معقدًا ويتم نقله عبر مجرى الدم إلى الكبيبات الكلوية حيث يتم ترشيحه واستئنافه من الأنابيب الكلوية. في خلايا الأنابيب ، يتم استقلاب مركب ميتالوثيونين - كادميوم ويطلق الكادميوم. هنا مرة أخرى ، يقوم القرص المضغوط بتنشيط التوليف المتزايد للميثاليون ، والذي يربط الكادميوم أكثر. يؤدي التراكم في الكليتين إلى تلف هذا العضو ، مما يؤدي إلى بروتينية. بسبب هذا الكادميوم المرتبط بالبروتين يتم إفراغه ببطء شديد للغاية ، يبقى عمر النصف للجسم حتى سنوات 30. لذلك ، يزيد محتوى الكادميوم من الولادة وينخفض مرة أخرى في عمر 50-60 سنة.
يدمر الكادميوم العظام أيضًا ، لأنه يؤدي في النهاية إلى تعبئة الكالسيوم. يتنافس الكادميوم في الأمعاء مع الكالسيوم في مواقع الربط على بروتين رابط الكالسيوم في الغشاء المخاطي في الأمعاء. بالإضافة إلى ذلك ، يمنع القرص المضغوط عملية إعادة تخليق 1,25-dihydroxycholecalciferol (الكالسيتريول) في خلايا الكلية الحبيبية. يعتبر 1,25-Dihydroxycholecalciferol ضروريًا لتنشيط تخليق البروتين المرتبط بالكالسيوم في الخلية المخاطية المعوية. باختصار ، يؤدي الكادميوم إلى انخفاض امتصاص الكالسيوم في الأمعاء والكلية ، وكذلك زيادة إفراز البول نتيجة لإطلاق الكالسيوم من العظام وبالتالي تدهوره.
في حالة التسمم الحاد بالكادميوم ، يمكن مساعدة إفراز الصفراوي من خلال إدارة البنسلامين أو ديميكابرول. فعال ، وراء علاج التسمم الحاد الكادميوم غير معروف.
الأعراض
- الإسهال وآلام في المعدة والقيء العنيف
- الفشل الكلوي
- كسور العظام
- الأضرار التي لحقت الجهاز العصبي المركزي
- الأضرار التي لحقت الجهاز المناعي
- اضطرابات التكاثر وربما حتى العقم
- الاضطرابات العقلية
- تلف الحمض النووي المحتمل والتسرطن
- فقدان حاسة الشم
روابط
→ الفئة: مركب الكادميوم
أكاسيد وهيدروكسيدات
- أكسيد الكادميوم
- هيدروكسيد الكادميوم Cd (OH) 2
هاليدات
- فلوريد الكادميوم CdF2
- كلوريد الكادميوم CdCl2
- بروميد الكادميوم CdBr2
- الكادميوم يوديد CdI2
chalcogenides
- كبريتيد الكادميوم CdS
- سيلينيد الكادميوم CdSe
- الكادميوم تيلورايد CdTe
مركبات أخرى
- كبريتات الكادميوم CdSO4
- نترات الكادميوم Cd (NO3) 2
- سيانيد الكادميوم Cd (CN) 2
- الكادميوم ستيرات مؤتمر نزع السلاح (C17H35COO) 2
سعر الكادميوم -> أسعار المعادن الاستراتيجية
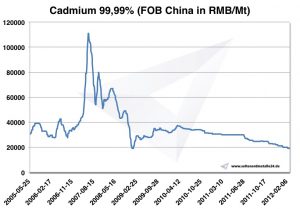
الرسم البياني Cadmium 2005-2012


